01 挑战:mrna 疫苗的“阿喀琉斯之踵”
尽管 mrna 疫苗具有合成快、成本低等优势,但目前的递送系统(如脂质纳米颗粒 lnp)仍面临诸多挑战:
缺乏靶向性:lnp 容易在肝脏富集,难以精准进入免疫反应的“司令部”——树突状细胞 (dcs)。
安全隐患:外源性载体可能引发过度的全身炎症反应(如“细胞因子风暴”)。
稳定性难题:极度依赖严苛的超低温冷链存储。
为了破解这些难题,研究者从导航定位(靶向)和动力增强(佐剂)两个维度出发,设计了全新的递送方案。
02 创新:compass 系统的多能“指南针”
研究团队利用滚环扩增技术 (rca)构筑了一根超长的单链 dna “骨架”,并巧妙地集成了多种功能模块,将其命名为指南针系统(compass, manganese-coordinated polyvalent aptameric system):
多价适体实现“器官-细胞”双级靶向:通过尺寸优化和多价适体精准识别能力,能够特异性靶向淋巴结组织中的树突状细胞表面的 dc-sign 受体,实现细胞级的精准导航。
锰离子 (mn²⁺):作为系统的“增压器”,锰离子不仅能促进 mrna 表达,更重要的是,它能激活 cgas-sting 信号通路 促进表达抗原的高效呈递。
dna骨架:通过碱基配对稳定装载 mrna,并利用致密的纳米结构抵抗核酸酶降解。
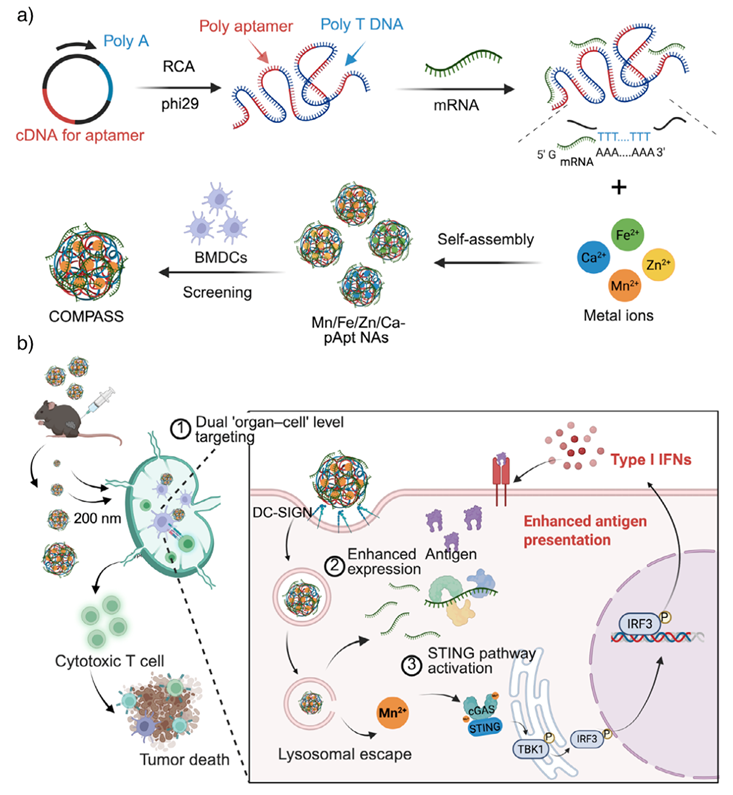
scheme.通过compass平台实现“器官-细胞”双级靶向递送mrna癌症疫苗,以诱导强效抗肿瘤反应。
03 核心优势:双重靶向,精准高效
1.“器官-细胞”双级靶向 compass 展现了精妙的定位能力:首先,通过优化纳米颗粒尺寸(约 200 nm),使其能顺畅地经淋巴管引流进入淋巴结(器官级靶向);随后,利用表面的多价适体精准锁定树突状细胞(细胞级靶向) 。
2. 锰离子助力“免疫觉醒” 与传统的佐剂不同,compass携带的 mn²⁺能在细胞内高效促进 mrna 的内体逃逸,并选择性激活 sting 通路 。这种激活方式能显著增强抗原呈递,诱导强大的 cd8 t 细胞免疫反应,像“精锐部队”一样精准清除肿瘤细胞 。
3. 媲美lnp 的效力,更优的安全性。在动物实验中,compass 表现出了与商业化 lnp(如 sm-102)相当的肿瘤预防和治疗效果 。令人振奋的是,相比 lnp 引起的局部中性粒细胞浸润和全身炎症因子上升,compass 几乎不引起明显的副作用,安全性表现极其优异 。
4. 告别超低温冷链 得益于 dna 纳米结构的稳定性,冻干后的 compass 疫苗可以在常温下储存超过三个月,其结构完整性和生物活性保持不变 。这意味着在偏远地区或冷链不发达地区,该疫苗同样具有巨大的应用潜力 。
04 展望
compass 平台的开发,不仅为 mrna 疫苗递送提供了一个可编程、高度集成的载体范式,也展示了“金属免疫疗法”在提升疫苗效力方面的巨大潜力。正如其名,compass 或将成为 mrna 癌症疫苗通往临床转化之路上的重要“指南针”。
05 论文信息:manganese-coordinated polyvalent aptameric system (compass) enables dc-targeted mrna/mn2 co-delivery for cancer immunotherapy.angewandte chemie international edition, 2026. doi: 10.1002/anie.202519216
上海交通大学医学院分子医学研究院刘学良副研究员为该论文的第一作者,谭蔚泓院士、杨宇研究员和刘庄教授为该论文通讯作者。该工作得到国家重点研发计划、国家自然科学基金等经费支持。
谭蔚泓:中国科学院院士,上海交通大学分子医学研究院院长。长期从事生物分析化学和化学生物学的研究。
杨宇:上海交通大学医学院研究员,博士生导师。专注于核酸技术与免疫治疗研究。
刘学良:上海交通大学医学院副研究员。专注于核酸药物靶向递送与精准免疫治疗的研究。





